Preparação de carbonato de cálcio esférico por cristalização e carbonização por reação de hipergravidade
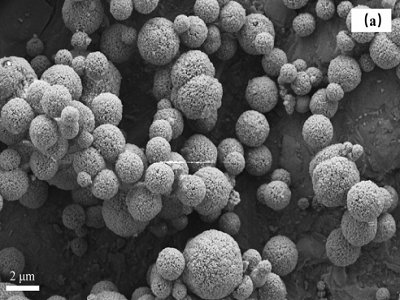
As formas comuns de carbonato de cálcio incluem principalmente forma irregular, forma de fuso, forma esférica, forma de floco e forma de cubo, etc. Diferentes formas de carbonato de cálcio têm diferentes campos de aplicação e funções. , solubilidade e grande área de superfície específica, etc., têm aplicações importantes nas áreas de plásticos, borracha, alimentos e fabricação de papel.
Atualmente, os principais métodos de preparação do carbonato de cálcio esférico são o método de metátese e o método de carbonização. Embora o método de metátese possa produzir carbonato de cálcio esférico com morfologia regular e boa dispersão, as matérias-primas desse método são caras e uma grande quantidade de íons impureza será introduzida, o que não é adequado para a produção industrial. O método de carbonização é o método mais utilizado na indústria. O método de carbonização tradicional é dividido principalmente no método de carbonização intermitente e no método de carbonização por pulverização contínua. Embora o método de carbonização tenha baixo custo e possa ser produzido em larga escala, o método tradicional de carbonização para preparação de carbonato de cálcio esférico apresenta problemas como distribuição de tamanho de partícula desigual e baixa eficiência de produção.
O método de cristalização por reação de hipergravidade é um novo método de preparação de nanomateriais, e sua essência é gerar enorme força centrífuga através de rotação de alta velocidade, simulando o ambiente de campo de hipergravidade. O rotor de empacotamento rotativo de alta velocidade no reator de hipergravidade bate o líquido em filamentos líquidos, gotículas ou filmes líquidos, e a área de superfície específica do líquido aumenta acentuadamente. 1 a 3 ordens de grandeza, os processos de micromistura e transferência de massa são bastante aprimorados, de modo que o tempo de reação é menor do que o método tradicional de carbonização e o produto tem as vantagens de tamanho de partícula pequeno, distribuição estreita de tamanho de partícula, alta pureza do produto , e morfologia mais regular. . Os reatores de hipergravidade são amplamente utilizados na preparação de nanomateriais devido à sua boa micromistura e efeitos de transferência de massa.
O carbonato de cálcio esférico é cultivado a partir de vaterita na maioria dos casos, mas a vaterita, como uma forma de cristal termodinamicamente instável, é difícil de existir de forma estável em um ambiente úmido e solução aquosa e requer alguns métodos especiais para obtê-la de forma estável. A pesquisa mostra que a introdução de NH4+ durante a reação de carbonização pode não apenas inibir a formação de calcita durante o processo de cristalização, e facilitar a transformação da forma cristalina de carbonato de cálcio em vaterita, mas também a atmosfera de NH4+ pode tornar a vaterita gerada existem de forma estável na solução.
Diferente do NH4+, os aminoácidos ácidos se dissociarão em solução e se combinarão com o Ca2+ para formar um molde de cristal semente. Sob a influência do molde de cristal de semente, o carbonato de cálcio resultante também aparecerá na fase de cristal metaestável e o aminoácido adequado. A introdução gerará funções específicas e modificará a morfologia durante a cristalização do carbonato de cálcio.
Usando ácido glutâmico de baixo custo e cloreto de amônio como aditivos, a preparação controlável de carbonato de cálcio esférico em um campo de hipergravidade foi estudada e os efeitos dos dois aditivos na síntese de carbonato de cálcio foram investigados. Os resultados mostraram que:
(1) Usando o método de cristalização e carbonização de reação de hipergravidade, o tamanho de partícula pode ser obtido sob as condições ideais em que ácido L-glutâmico e cloreto de amônio são adicionados a 4% e 20% de hidróxido de cálcio, respectivamente, e o fator de hipergravidade é 161,0. Carbonato de cálcio vaterita puro com alta esfericidade de cerca de 500nm.
(2) Antes do início da reação, o ácido L-glutâmico e os íons cálcio na solução formam um molde, que afeta a nucleação e o crescimento do carbonato de cálcio, e o NH4+ abundante na solução durante a reação proporciona um bom ambiente para a formação de carbonato de cálcio. vaterita, O corte de alta velocidade do líquido pelo reator de hipergravidade evita a possibilidade de revestimento excessivo de matérias-primas de hidróxido de cálcio e realiza a preparação controlável de carbonato de cálcio esférico.
